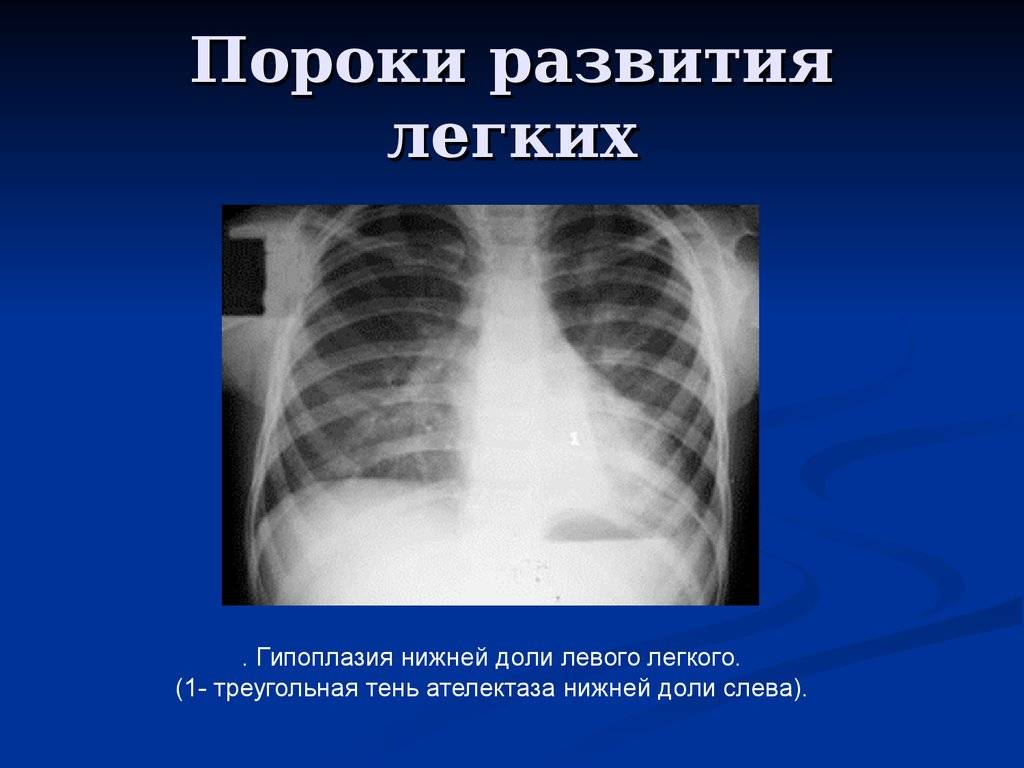
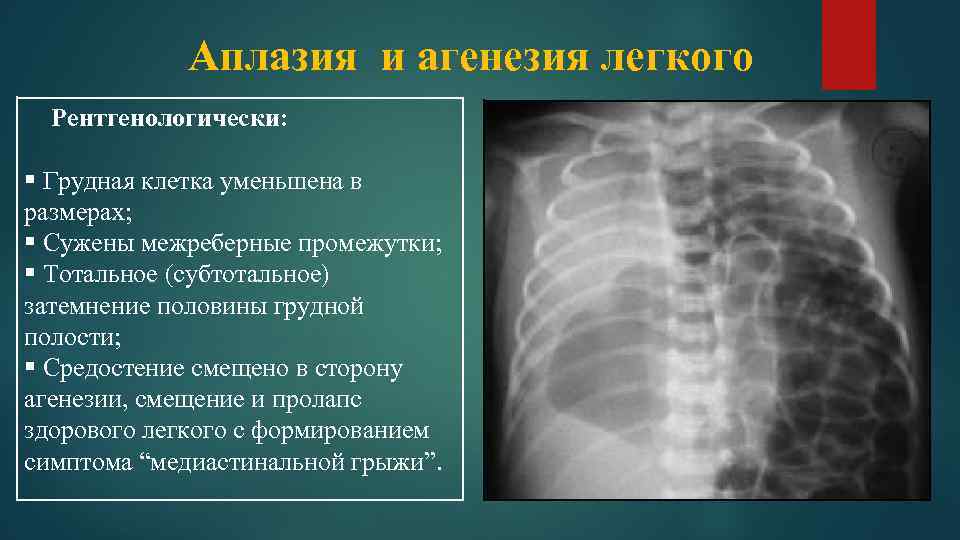
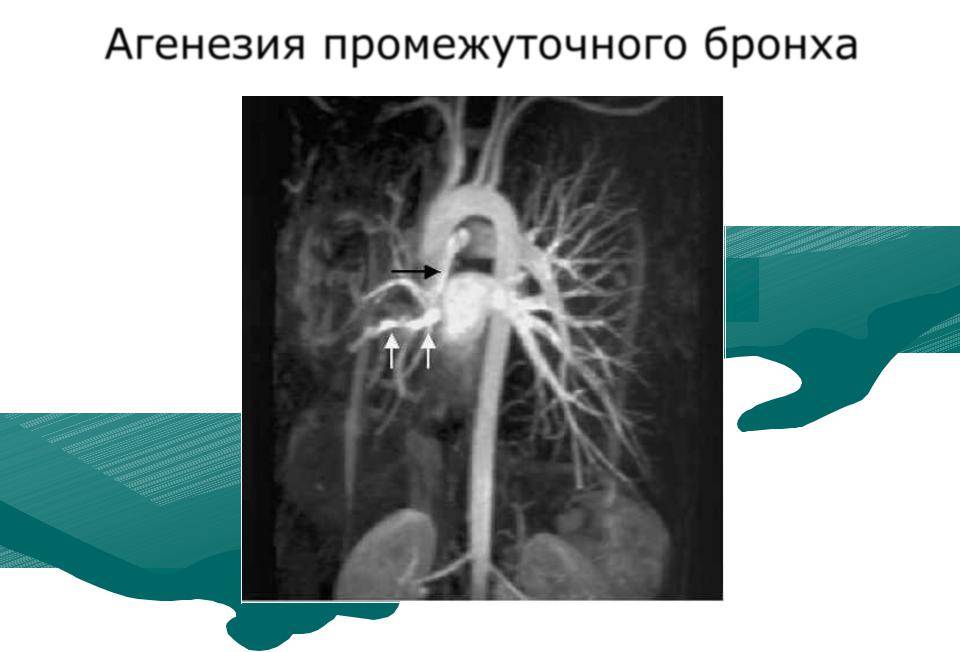
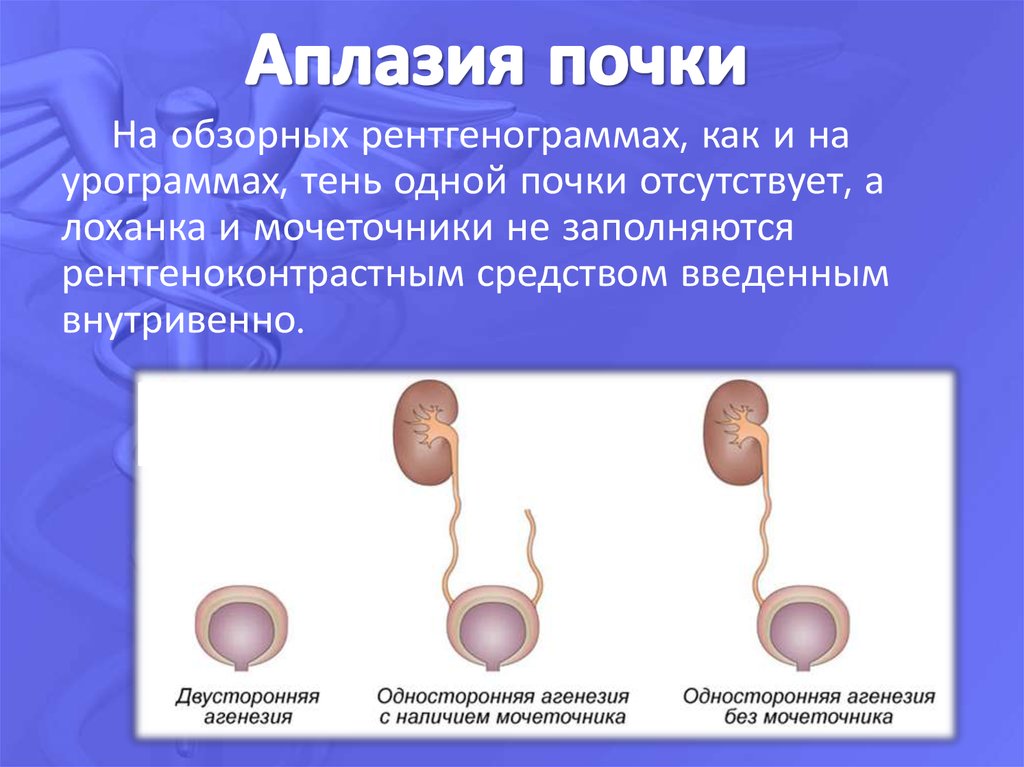
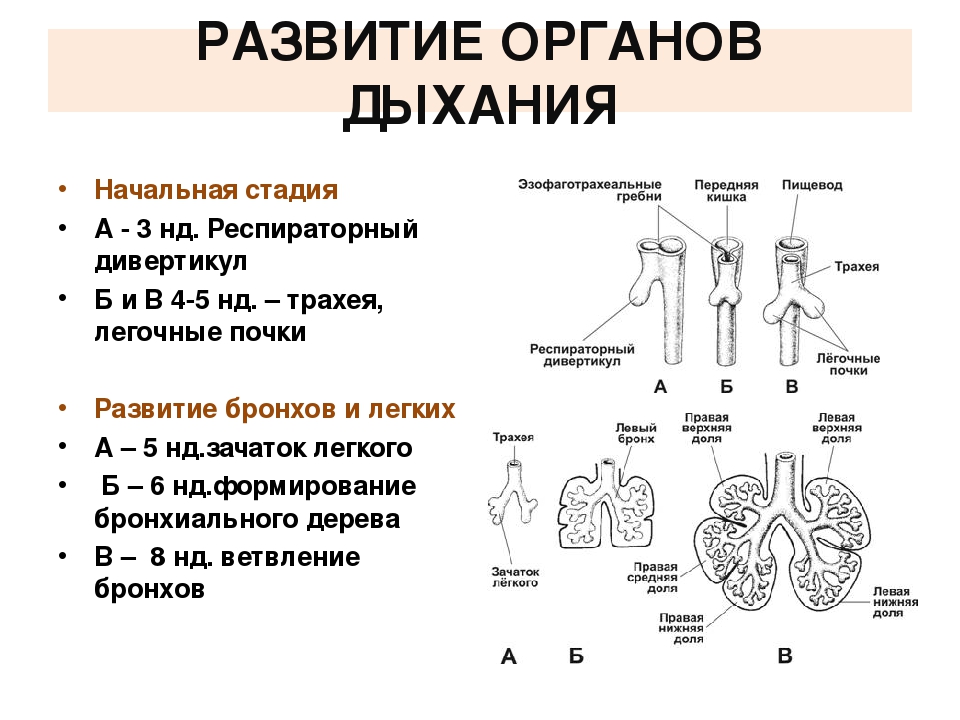
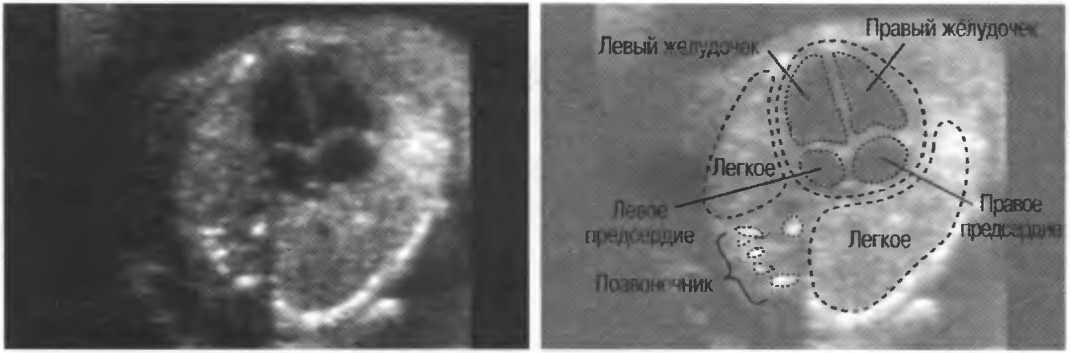
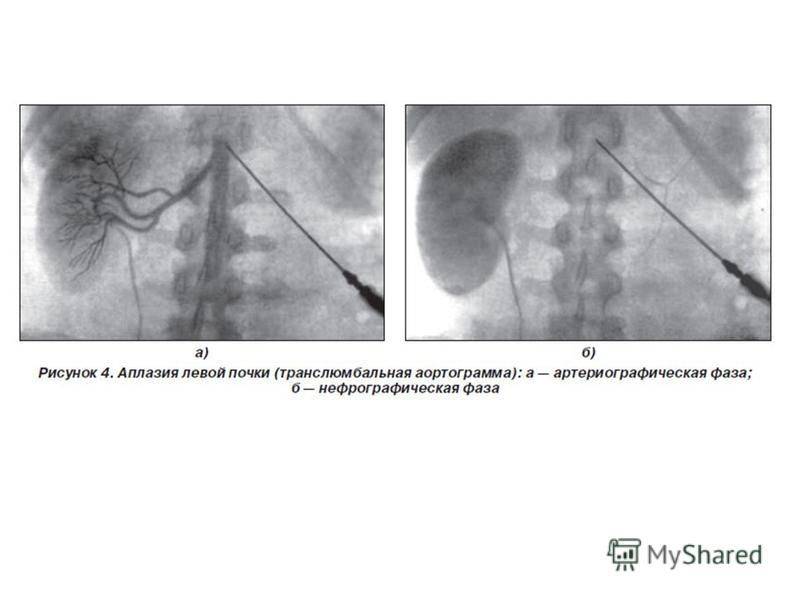
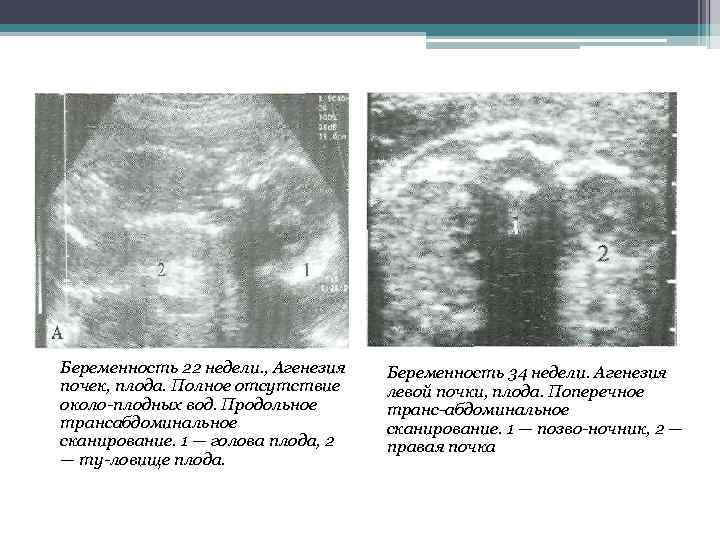
Введение
Зрелость легких плода имеет жизненно важное значение для выживания новорожденных детей и определяет их внеутробную жизни. Респираторный дистресс синдром (РДС) и связанные с ним осложнения вызывают смерть новорожденных в 28% случаев. Однако, широкое пренатальное применение глюкокортикоидов уменьшили заболеваемость РДС
Точная оценка дородовой зрелости легких плода, особенно во время беременности с высокой степенью риска, имеет решающее значение для улучшения неонатального выживания
Однако, широкое пренатальное применение глюкокортикоидов уменьшили заболеваемость РДС. Точная оценка дородовой зрелости легких плода, особенно во время беременности с высокой степенью риска, имеет решающее значение для улучшения неонатального выживания.
Идентификация фосфолипидов в амниотической жидкости, включая фосфатидилглицерол, фосфатидилэтаноламин и соотношение лецитин/сфингомиелин (L/S соотношение), является основным методом определения дородовой зрелости легких, который широко применяется в медицинской практике.
С 1980-х годов многие исследовали использование ультразвука для контроля зрелости легких плода. Исследование эхогенности легких плода, дыхательноподобных движений плода, допплеровского спектра, связанного с назальным потоком жидкости при дыхательноподобных движениях плода (BRNFF) и данные объема легких связаны с анализом зрелости легких плода, однако до сих пор нет единого набора сонографических критериев.
В Китае для ультразвукового исследования развития легких плода нет нормативного диапазона показателей, как определения объема легких, например. Таким образом, данное исследование было проведено (I) для оценки возможности и точности ультразвуковых показателей оценки зрелости легких плода; (II) установления границ нормы объема легких плода и сравнения эхогенности легких к эхогенности печени плода (FLLIR) в китайской популяции.
Риски для недоношенных деток или при многоплодной беременности
Незавершенное созревание легочных структур плода сопряжено с определенными рисками, которые особенно выражены у новорожденных, появившихся на свет до необходимого срока или при многоплодной беременности.
У недоношенных малышей основной причиной летального исхода после рождения является респираторный дистресс синдром, причина которого – недозревшие легкие. Поскольку сурфактант начинает синтезироваться лишь к концу 2 триместра, считается, что альвеолы у таких малышей вплоть до 34-36 недели недоразвиты, не существуют как полноценные структуры. Газообмен в этих условиях резко понижен и велика вероятность слипания альвеол при рождении плода.
При вынашивании женщиной нескольких плодов, причиной для переживаний специалистов выступает то, что у обоих плодов возможна задержка развития, или же один плод будет развиваться активнее, подавляя другой. В таком случае нередко формируется ситуация, когда из нескольких родившихся малышей, только один способен к нормальному дыханию вне утробы, а другим необходимо оказание помощи.
На какой неделе беременности ткань приобретает полноценный вид
Завершается развитие легочной ткани только к моменту 36 недели гестации. К этому периоду количество сурфактанта становится достаточным, для нормального дыхания ребенка, покинувшего материнскую утробу. При рождении плода раньше времени, недостаточный уровень этого вещества сопряжен с дыхательными нарушениями, требующими определенной врачебной помощи.
Обращаетесь ли Вы при лечении к специалистам?
Да, так быстрее, чем искать, то что может быть симптомом 10-20 болезней. 38.71%
Обычно не обращаемся, убираем симптомы и все проходит само. 21.77%
Лечимся только сами, да плохо заниматься самолечением, но бывает это лучше и быстрее чем обратиться к врачу(запись, очереди, непонятные назначения), быстрее сам себе поможешь. 39.52%
Проголосовало: 496
Диагностика врожденной патологии
В наше время, благодаря достижениям современной медицины, возможна ранняя диагностика врожденной патологии во внутриутробном периоде. Информация, полученная после диагностики врожденных пороков, необходима для принятия решения о дальнейшей тактике ведения пациентки:
- срочного лечения врожденного порока;
- проведения родов в специализированных учреждениях для своевременного лечения врожденных пороков;
- прерывание беременности при невозможности лечения врожденного порока и нарушениях, несовместимых с жизнью.
Стоит отметить, что терапия детской врожденной патологии различается по степени тяжести и природе порока. По данным статистики, врожденные патологии плода в 25% случаев приводят к гибели малыша в течение 1 года жизни. В 25% врожденные пороки развития у детей приводят к умственным и физическим отклонениям. И только в 5% случаев есть возможность проведения лечения детской врожденной патологии.
Диагностика врожденной патологии заключается в проведении прямых (инвазивных и неинвазивных) и непрямых способов исследования.
Непрямые методы диагностики врожденных пороков: анализы крови на АФП, ХГЧ, гормоны, иммунологические, серологические, генетические тесты и т.п. На основании результатов этих исследований можно предположить наличие или высокий риск развития врожденных пороков плода. Особое значение в диагностике врожденной патологии имеет определение уровня АФП и ХГЧ, так как отклонения от нормы часто предполагают формирование врожденной патологии плода, в частности нервной системы.
Помимо этих способов исследования, все беременные проходят неинвазивные прямые методы диагностики врожденных пороков в плановом порядке: УЗИ, допплерометрия, КТГ. УЗИ проводится 3 раза в течение всего срока беременности, но при необходимости назначают дополнительные процедуры. Так как к 19-20 неделе уже сформированы практически все органы и системы, то видны на УЗИ врожденные пороки развития плода в 80-86% случаев. Одна из разновидностей УЗИ – допплерометрия, позволяющая оценить параметры кровообращения. При этом признаки врожденных пороков развития на УЗИ определяются в ранние сроки беременности.
На 28-30 неделе беременности и во время родов беременным проводят КТГ, этот метод позволяет оценить характер сердечных сокращений плода (при помощи УЗ датчика) и схваток, а также определить вероятность осложнений родового и послеродового периода. Стоит отметить, что КТГ позволяет определить УЗ признаки врожденных пороков развития сердца и системы кровообращения, а также врожденные пороки центральной нервной системы. Если результаты неинвазивной диагностики врожденных пороков плода неудовлетворительны, то прибегают к дополнительным инвазивным методикам для изучения генетического материала плода (амниоцентезу, плацентоцентезу, хорионцентезу, забору крови пуповины, биопсии ворсин хориона).
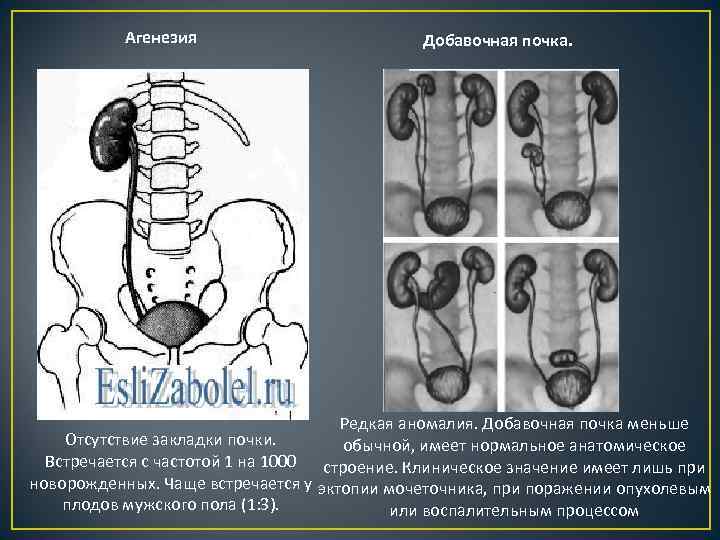
Двусторонняя агенезия:
- Редкий врожденный порок (полное отсутствие почек) встречается с частотой примерно 1:4000.
- Считается фатальным пороком, поражает плоды мужского пола до 2,5-3 раз чаще чем женского.
- Чаще всего ее сопровождают пороки сердца, VATER-синдром, аномалии пальцев рук и женских половых органов.
- Двустороннюю агенезию почек подозревают, когда во втором триместре УЗИ не выявляет почки и плодный пузырь, что сопровождается выраженным маловодием (недостаток околоплодных вод).
- Прогноз при двусторонней агенезии неблагоприятный. Плоды, лишенные почек, обычно доживают до родов, так как внутриутробно функцию почек выполняет плацента. Но все же, новорожденные умирают вскоре после рождения либо от гипоплазии легких, либо от синдрома Поттера.
- Последовательность Поттера представляет собой последовательность врожденных дефектов, чаще всего вызванную двусторонней агенезией почек и ассоциированным маловодием или безводностью. Проявление данного синдрома: деформация конечностей, контрактуры суставов, уменьшение окружности грудной клетки, лицо Поттера (плоский нос, широко расставленные глазные яблоки, маленькая нижняя челюсть и большие, низко посаженные уши). Не совместима с жизнью.
Диагностика
Для качественного диагностирования порока необходимо проконсультироваться у пульмонолога насчёт проведения комплексного обследования. Подозревают наличие пороков у тех пациентов, которые с детства страдают хроническими заболеваниями лёгких и бронхов.
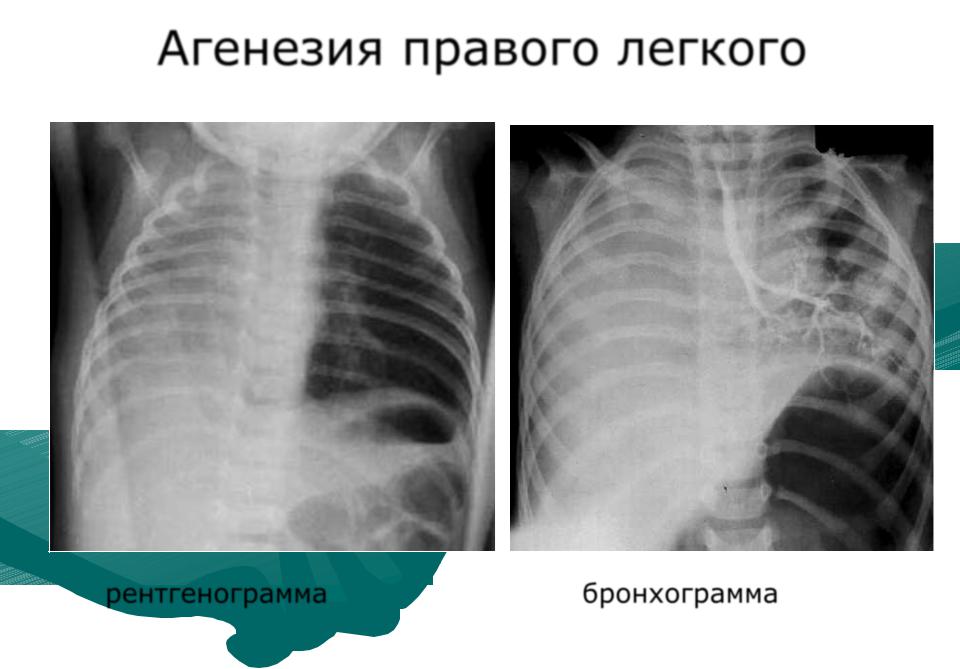
Наиболее эффективные методики обследования – бронхологическая и рентгенологическая.
Рентген лёгких и компьютерная томография позволяют выявить наличие порока даже при отсутствии клинической симптоматики, эти процедуры обеспечивают информацией об изменениях в бронхиальном и сосудистом рисунках, указывают на повышение прозрачности, смещение органов средостения, обнаруживают обратную топографию лёгких и др.
Бронхоскопия, а также бронхография позволяют оценить анатомические особенности строения бронхов и трахеи, обнаружить свищи, стеноз и другие дефекты строения, подтвердить изменения в бронхиальном дереве.
Если есть подозрение на пороки развития сосудов лёгкого, то требуется ангиопульмонография.
Клиническая картина
Неразвитость тазобедренных суставов у новорожденных иногда обнаруживается в условиях роддома при первом осмотре детского ортопеда. Но в отличие от дисплазии незрелость ТБС не проявляется выраженной симптоматикой, особенно в течение первых дней жизни ребенка. Признаки замедленного окостенения и неправильного формирования сочленений обычно возникают после 3 месяцев. Что могут заметить родители или педиатр при очередном осмотре:
- укорочение бедра;
- снижение мышечного тонуса;
- асимметричное расположение кожных складок;
- возникновение препятствия при попытке отведения сочленения;
- характерный щелчок при отведении ТБС.
Чем раньше диагностирована патология, тем быстрее и успешнее проходит терапия. Обнаружить недоразвитость позволяют внешний осмотр, жалобы родителей, проведение функционального тестирования. Подтвердить диагноз помогают результаты ультразвукового, рентгенологического исследований. Хотя рентгенография считается самым информативным методом, ее проведение противопоказано детям до 3 месяцев. Степень зрелости ТБС устанавливается по параметрам ультразвуковой классификации Графа. Например, тип 2а по Графу – это незрелый диспластичный сустав.
Окостенение бедренных головок происходит примерно в возрасте 7 месяцев у девочек, 9 — у мальчиков. Если лечение незрелости тазобедренных суставов проводится до достижения ребенком полугода, то в дальнейшем они формируются в пределах нормы.
| Формы недоразвития тазобедренных суставов | Краткое описание |
| Ацетабулярная форма | Так называется врожденное недоразвитие вертлужной впадины у новорожденных. Для него характерны изменение централизации бедренной головки и повышенная эластичность связок. Отклонения незначительны, легко корректируются лечебными массажем и гимнастикой. В первые месяцы жизни подобное состояние той или иной степени выявляется у большинства младенцев. Станет ли оно предпосылкой для неправильного формирования ТБС, позволяют установить только последующие обследования, которые обычно проводятся через месяц |
| Диспластические изменения проксимального отдела бедренной кости | Такая врожденная форма недоразвития выявляется при измерении шеечно-диафизарных углов. Параметр рассчитывается по линиям, объединяющим центры шеек и головок костей, и диафизарным линиям. У детей старше 3 месяцев недоразвитие бедренных головок устанавливается по рентгенографическим изображениям |
| Ротационное недоразвитие | Нарушение развития, для которого характерны изменения углов между осями тазобедренных и коленных суставов в горизонтальных плоскостях. При отклонении полученных значений от нормы (у новорожденных – около 35°) диагностируется нарушение центрирования ТБС в вертлужной впадине |
ПАТОЛОГИЯ ПЕРИНАТАЛЬНОГО ПЕРИОДА
Перинатальный
период – период с 22-й полной недели (154-го дня) внутриутробной
жизни плода до семи полных суток после рождения ребёнка.
Неонатальный период начинается с момента рождения и заканчивается через 28 дней жизни ребёнка.
Живорождение –
полное изгнание или извлечение продукта зачатия из организма матери
независимо от продолжительности беременности, если плод имеет при
рождении любой из четырёх признаков жизни: самостоятельное дыхание,
сердцебиение, пульсацию сосудов пуповины, произвольные движения
мускулатуры.
Мертворождение – смерть продукта
зачатия, наступившая до его полного изгнания или извлечения из организма
матери. Смерть, наступившая до начала родовой деятельности, называют
антенатальной, смерть во время родов – интранатальной. Смерть
плода, наступившую ранее 28 нед беременности, делят на раннюю (до
20 нед) и позднюю (21-28 нед).
Младенческая смертность – число детей, умерших в возрасте до 1 года на 1000 живорождённых.
Неонатальная
смертность – число детей, умерших в возрасте до 28 суток на
1000 живорождённых. Выделяют следующие виды:
∨ ранняя неонатальная смертность – смертность новорождённых в течение первых 7 сут жизни;
∨ поздняя неонатальная смертность – смертность новорождённых с 8-го по 28-й полный день жизни.
Перинатальная
смертность – число рождённых мёртвыми и умерших в первые
6 сут после рождения на 1000 рождённых живыми и мёртвыми.
Показатели перинатальной смертности значительно неодинаковы в разных
странах – от 12 до 50‰. В России этот показатель в 1999 г
составил 14,3‰.
3.Симптомы и диагностика
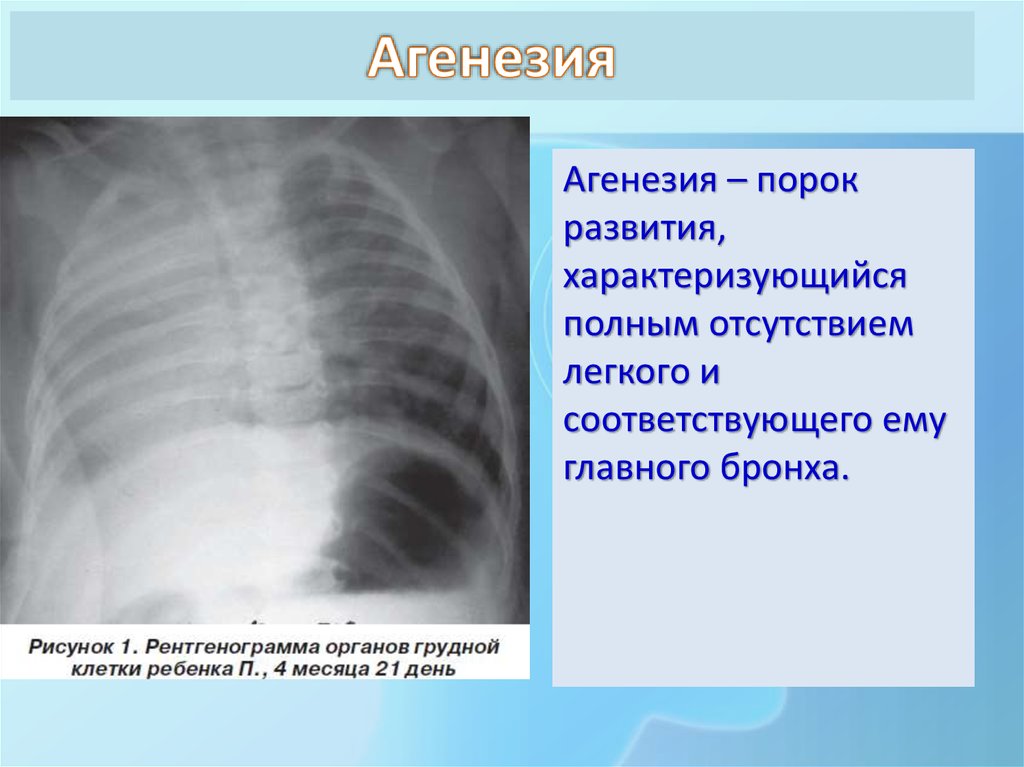
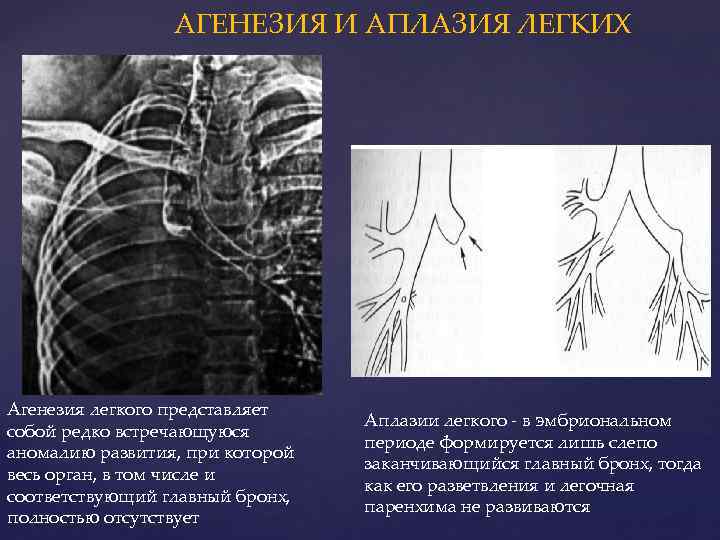
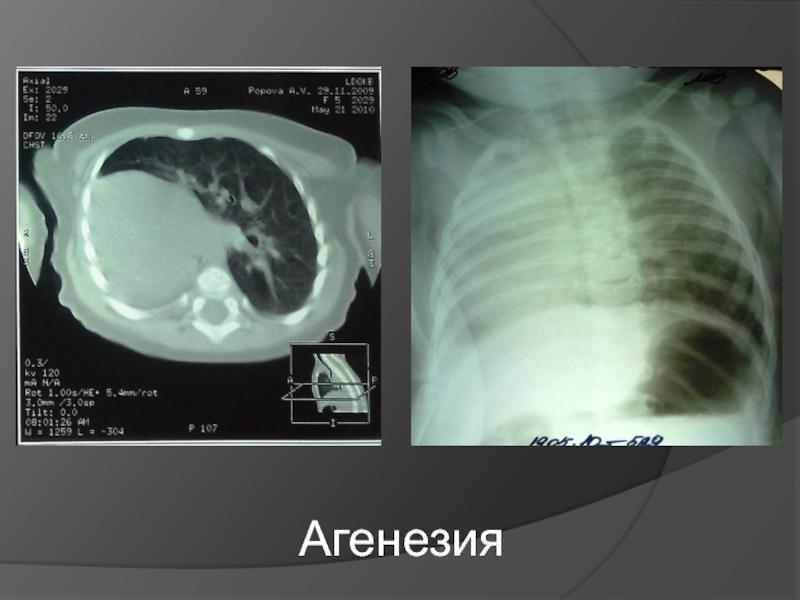
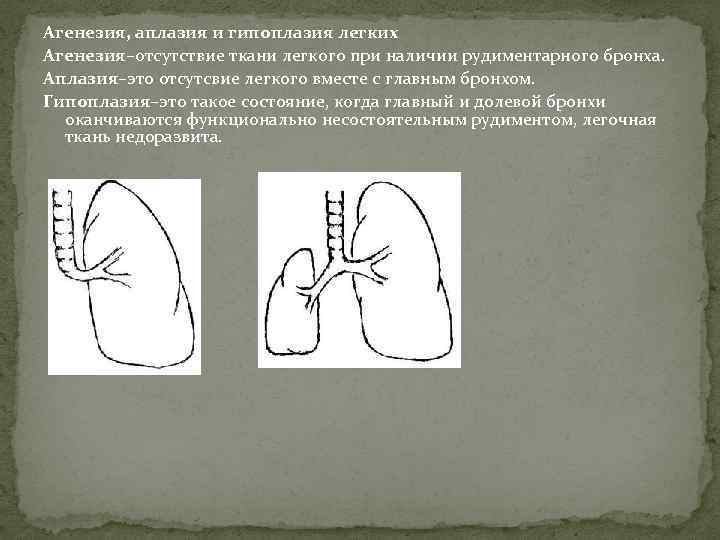
Двусторонняя агенезия несовместима с жизнью.
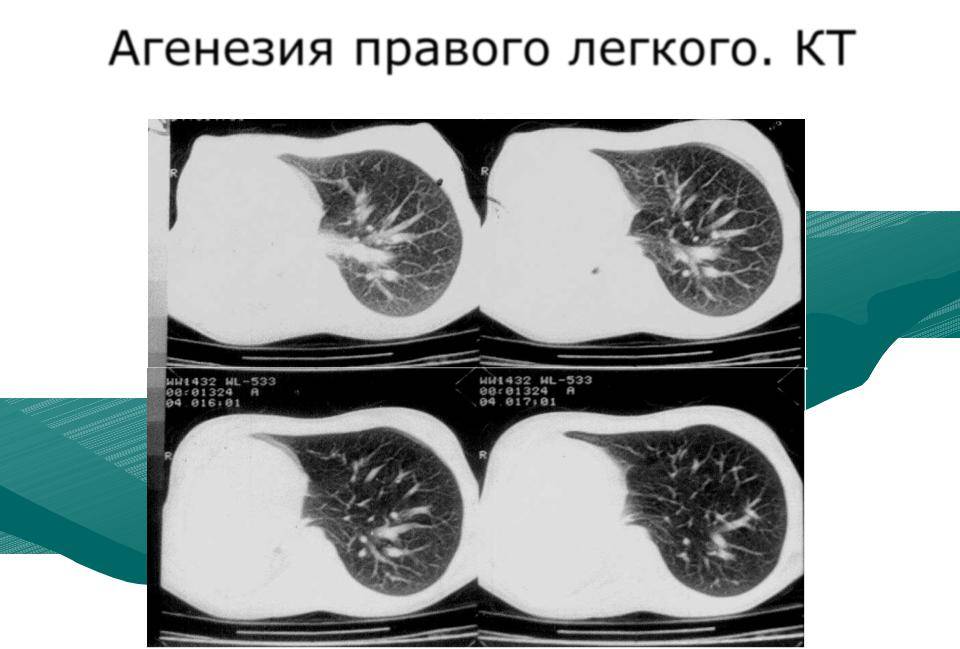
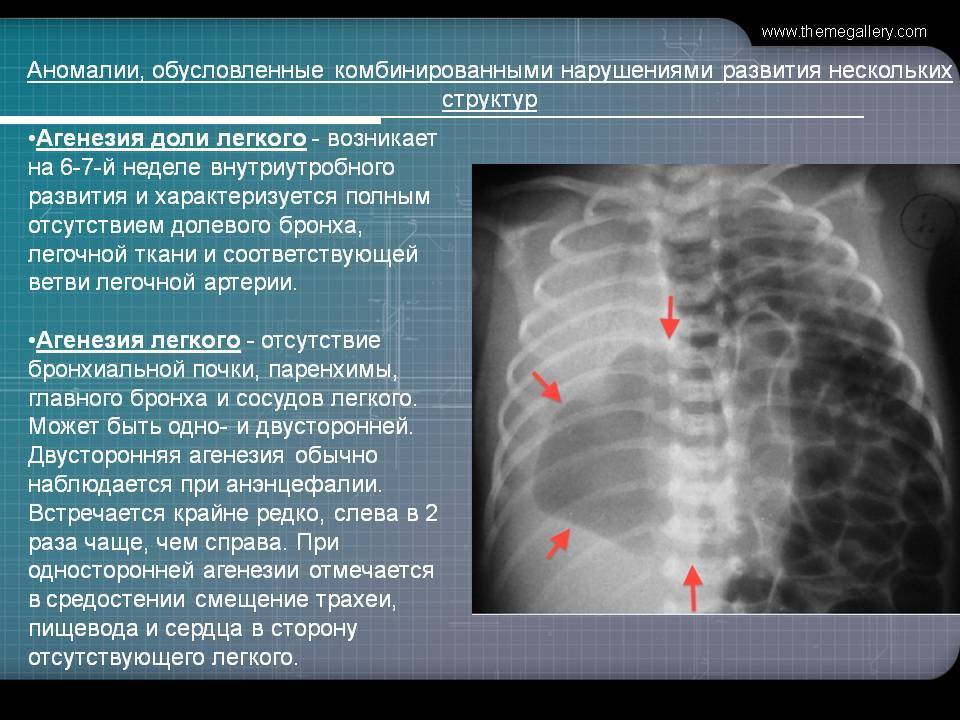
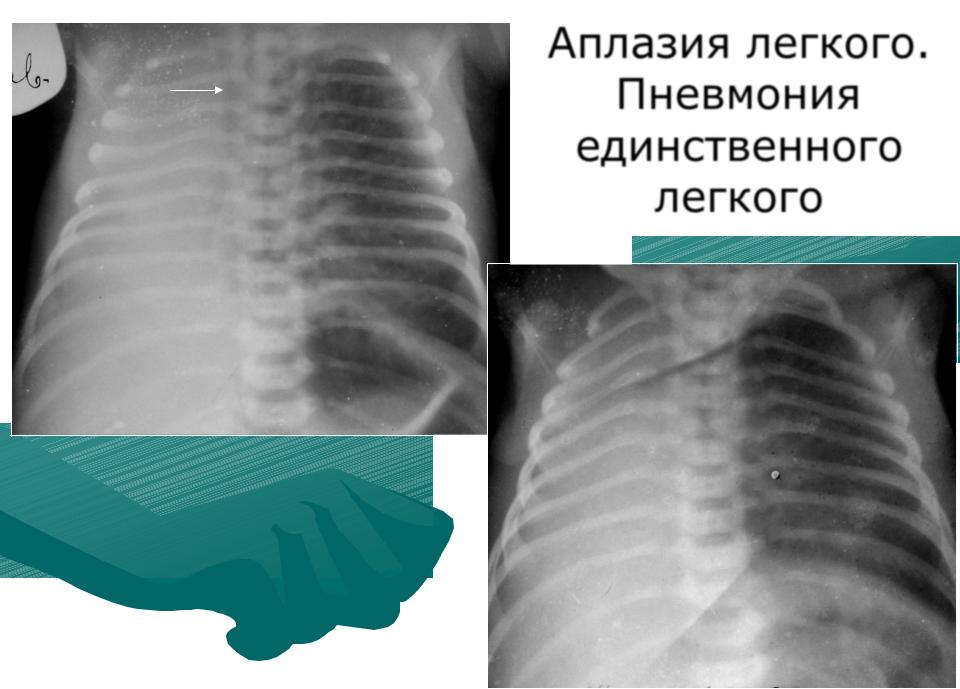
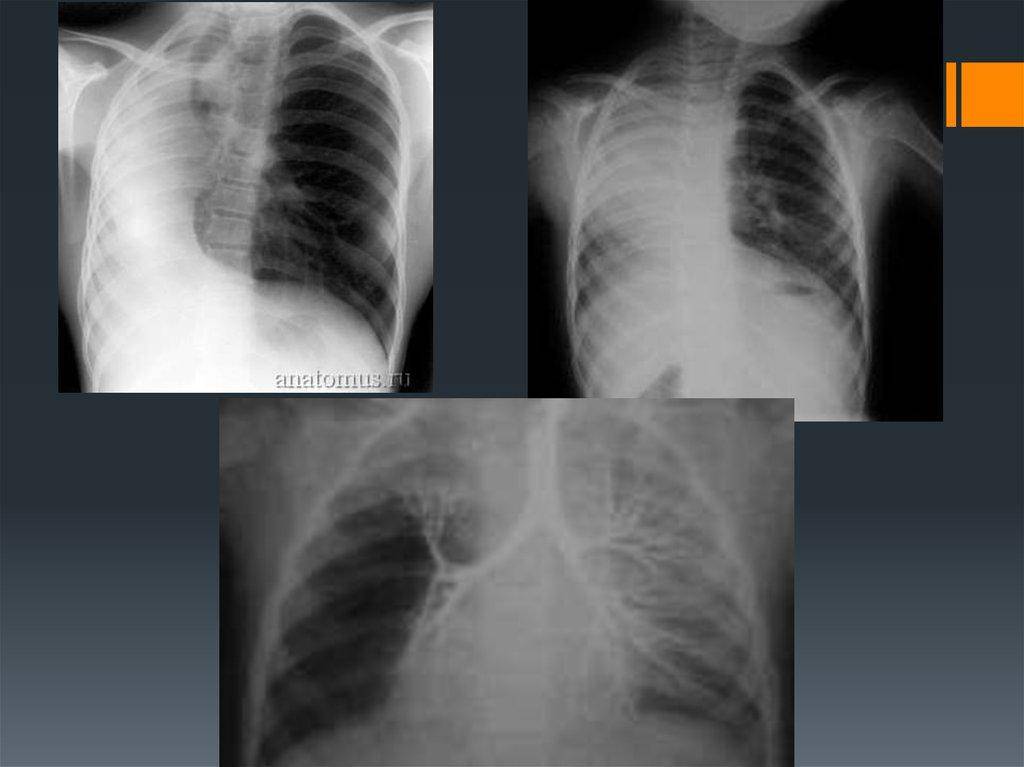
При односторонней чаще отсутствует левое легкое; нередко такая аномалия сочетается с другими пороками внутриутробного развития. Агенезия/аплазия легкого может длительное время протекать мало- или бессимптомно, однако она проявляется асимметрией дыхания при аускультации и притуплением звука при перкуссии. Смещение органов внутри грудной клетки, компенсаторное увеличение сохранного легкого может приводить к ее деформациям. В тяжелых осложненных случаях острая дыхательная недостаточность возникает непосредственно после рождения, быстро нарастает и заканчивается летально.
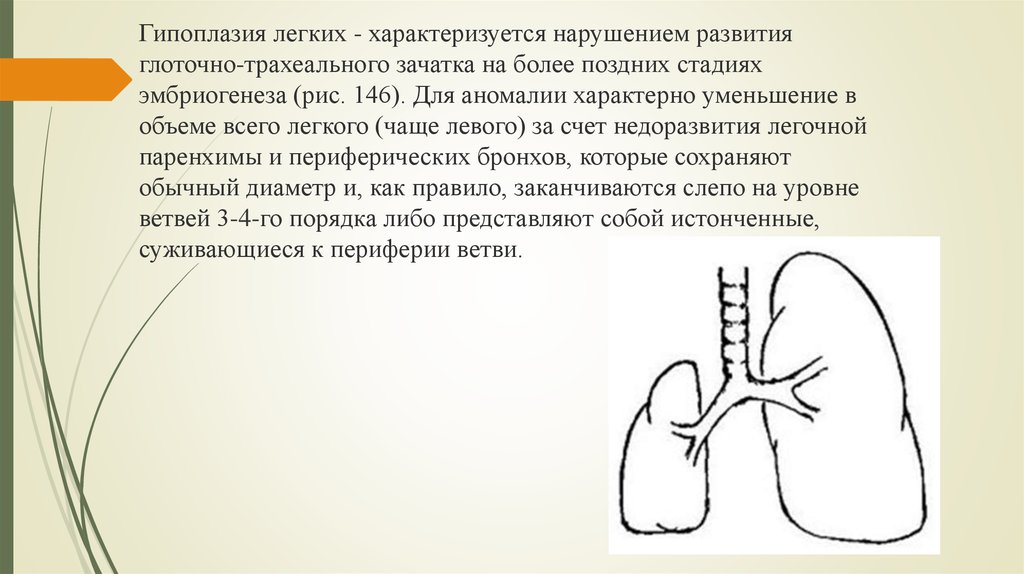
Гипоплазия клинически делится на две формы, простую и кистозную (врожденный поликистоз), при которой, как правило, имеет место хронический воспалительный процесс в дыхательной системе (с соответствующей симптоматикой).
Следует понимать, что столь серьезные аномалии, как агенезия, аплазия или гипоплазия легкого не может не сказываться на эффективности дыхания и газообменных процессов. В той или иной степени (от субклинической до критически тяжелой) дыхательная недостаточность присутствует во всех случаях; наличие порока отражается на качестве жизни, внося существенные ограничения, и является одним из факторов сокращения ее продолжительности.
Агенезия и гипоплазия легкого может быть предположительно диагностирована уже при стандартном осмотре и аускультации. Такие пороки развития легко подтверждаются рентгенологически. Как правило, назначается также ангиопульмонография.
Что означает степень зрелости легких у ребенка
Возможность малыша жить вне материнской утробы определяется, в том числе, степенью зрелости его легких и их способностью к поддержанию достаточной оксигенации организма. По мере того, как происходит развитие всех систем и органов плода, меняется и анатомия легочной системы. Эти изменения касаются также физиологических и биохимических параметров органа.
В процессе развития ребенка формируется определенное вещество, которое называется сурфактант. Именно по нему определяют степень зрелости легких плода. Он образуется, начиная с 24 недели беременности, а с 36-й его количество стремительно увеличивается.
Сурфактант — это вещество, которое способствует тому, чтобы при первом вдохе ребенка после рождения альвеолы не слипались. Еще одна из его функций — защитная, благодаря сурфактанту патогенные микроорганизмы не могут проникнуть в альвеолы, а их полости он предохраняет от проникновения жидкого компонента плазмы.
Наблюдение за созреванием легочной ткани младенца начинают проводить с 33-й недели беременности. Для того чтобы определить степень зрелости этих органов ребенка, специалисты используют несколько методов исследования, наиболее информативным из которых считается анализ околоплодных вод и определение процента концентрации в них фосфолипидов. Своевременное обследование позволяет оценить, насколько правильно формируются легкие плода, и выявить отклонение от нормативов на ранних сроках.
Профилактика и лечение
С целью предупредить развитие умственной отсталости еще в утробе у матери беременным женщинам, которые обладают неблагоприятным анамнезом (физиологические показатели, предрасположенность) рекомендовано более тщательное обследование. Под особое наблюдение врачи ставят женщин, которые в период беременности болели вирусными заболеваниями.
К поражению головного мозга могут привести родовые травмы, полученные новорожденными, а также перенесенные ими в раннем возрасте инфекционные заболевания.
Дитя с легкой умственной отсталостью, имеет возможность развиваться и обучаться в пределе своих биологических возможностей. Данная патология неизлечима, но своевременная и грамотная ее коррекция даст возможность стать для такого человека полноценным членом общества, хоть и с ограниченными способностями. Особую роль в данном случае играет окружение и восприятие. Несомненно, что такие люди требуют к себе повышенного внимания.
Для олигофренов необходим тесный контакт с близкими людьми, педагогами, врачами, психологами. Специализированные учреждения для детей с проблемами развития психики врач подбирает с учетом возможностей и способностей ребенка. Дополнительно психотерапевт может назначить медикаментозную поддержку с использованием фармакологических препаратов. Хороший результат показывают лечебно-воспитательные мероприятия, трудовое обучение умственно отсталых.
Всегда важно помнить, что любое психическое заболевание – это еще не приговор. Главное – вовремя обратиться к специалисту, который поможет сделать пребывание в обществе максимально комфортным и плодотворным для больного
В случае легкой олигофрении специалисты ставят относительно благоприятный прогноз. Это касается случаев, не отягощенных сопутствующими психопатологическими и соматоневрологическими расстройствами. Люди с такими отклонениями вполне способны освоить определенные виды профессий, могут приспособиться к самостоятельному проживанию и даже создают семьи.
Лечение
Для выбора оптимального метода лечения необходимо записаться на приём к торакальному хирургу или к пульмонологу. Характер терапии определяется общим состоянием пациента, степенью проявления патологии, прогнозами на лечение. Немедленное хирургическое вмешательство требуется в следующих случаях выраженной дыхательной недостаточности:
- Лобарная эмфизема;
- Агенезия лёгких;
- Аплазия;
- Стеноз бронхов или трахеи;
- Трахеопищеводный свищ.
Наиболее распространённая методика лечения бронхоэктазов – удаление изменённой области органа, однако возможно и медикаментозное лечение, что зависит от количества рецидивов и объёма изменённой лёгочной ткани.
Также важно проведение консервативного лечения, которое позволяет предупредить развитие гнойных процессов: массаж грудной клетки, бронхоальвеолярный лаваж, ЛФК, ингаляции и др
Диагностика Бронхолегочной дисплазии:
Для диагностики важны данные анамнеза. На бронхолегочную дисплазию у ребенка указывает рождение на сроке до 32 недель, проведение ИВЛ в периоде новорожденности. Также важны клинические данные. У ребенка есть потребность в кислороде (дети до 28 дней жизни).
Врачи проводят осмотр, чтобы зафиксировать одышку и учащенное дыхание. Также применяют обязательно аускультацию легких, выслушивая дыхательные шумы и влажные хрипы. Рентгенограмма показывает замещение легочной ткани соединительной, что является типичным признаком отека и фиброза. В некоторых случаях прибегают к консультации пульмонолога.
СИНДРОМ ВНЕЗАПНОЙ СМЕРТИ МЛАДЕНЦЕВ
Синдром внезапной смерти младенцев – внезапная гибель ребёнка моложе 1 года в случае, когда причины гибели неясны даже после тщательного посмертного исследования. Больной ребёнок может умереть внезапно при отсутствии клинически выраженных признаков заболевания.
Возможные причинывнезапной смерти: инфекционные болезни, врождённые пороки сердца, нарушения сердечной проводимости, врождённые и приобретённые нарушения ЦНС с судорогами и приступами апноэ, опухоли мозга, заболевания и состояния, протекающие с гипогликемией, механическая асфиксия, отравления, травмы. Если при патологоанатомическом исследовании или сборе анамнеза выявляют признаки перечисленных заболеваний и состояний, то такие случаи не относят к синдрому внезапной смерти ребёнка.
Частота синдрома внезапной смерти составляет 1-5 случаев на 1000 живорождённых. В настоящее время частота имеет тенденцию к росту, так как очень высокий риск развития синдрома внезапной смерти отмечают у глубоко недоношенных детей, число их растёт в связи с успехами выхаживания. Пик частоты синдрома – период 2-6 мес.
Выделяют факторы риска со стороны матери и плода.
• Факторы риска со стороны матери: возраст моложе 20 лет, низкое социально-экономическое положение, короткий промежуток между беременностями, многоплодная беременность, курение, приём наркотиков и алкоголя, инфекции мочевых путей во время беременности.
• Факторы риска со стороны плода: недоношенность, низкая масса тела при рождении, мужской пол, внутриутробная гипоксия, нарушение терморегуляции (гипо- и гипертермия), предшествующие приступы апноэ, перенесённая незадолго до смерти респираторная инфекция.
Этиология и патогенез Единой точки зрения на этиологию и патогенез синдрома внезапной смерти не существует. Наиболее распространена теория апноэ, согласно ей остановка дыхания – основной механизм наступления смерти. Апноэ центрального генеза связывают с незрелостью дыхательных центров новорождённого, его повышенной чувствительностью к гипоксии, гиперкапнии, изменению температуры тела и другим факторам. Кроме того, установлено, что у детей до 6 мес затруднено переключение носового дыхания на ротовое, особенно во время сна. Поэтому при отёке или гиперсекреции слизи в носоглотке может возникнуть механическая обструкция дыхательных путей.
Классификация заболевания
Специалисты выделяют четыре типа указанного заболевания, которые зависят от тяжести течения патологии вышеуказанной болезни.
Классификация легочной гипертензии:
- легочная гипертензия 1 степени характеризуется тем, что пациент не испытывает никаких неприятных ощущений при умеренной двигательной активности, у него не наблюдается одышка, отсутствуют болевые ощущения в районе груди, нет слабости или сильной усталости;
- умеренная легочная гипертензия представляет собой картину, когда при небольшом увеличении привычной физической активности отсутствуют вышеперечисленные признаки заболевания, а при значительном увеличении двигательной активности появляется легкое головокружение, одышка, пациент быстро устает;
- в третьей степени легочной гипертензии даже незначительная нагрузка вызывает болевые ощущения, головокружение и одышку;
- четвертая степень заболевания характеризуется тем, что вышеуказанные признаки могут проявляться у пациента даже в состоянии покоя.
Также легочная гипертензия имеет классификацию по течению указанного заболевания легких, она подразделяется на течение в остром и хроническом периоде. Острая форма чаще наступает в результате перенесенного инфаркта миокарда либо гипертонического криза, также спровоцировать острую стадию может в результате тромбэмболии легочной артерии и т.д. Хроническая гипертензия развивается на фоне повышения кровеносного давления в левом предсердии, в результате обструктивных легочных заболеваний, а также по иной причине, вызывающей сужение артерии в легких.
2.Причины
Предполагается, что причины возникновения внутриутробных бронхолегочных пороков не отличаются принципиально от тератогенных факторов вообще. В литературе наиболее часто описываются такие экзогенные, внешние тератогенные воздействия, как травма (механическая, температурная, лучевая, химическая), инфекция, курение и употребление алкоголя в период гестации, продолжительный прием некоторых медикаментов. К эндогенным, внутренним причинам относят наследуемые и первичные хромосомные и генные мутации.
Однако установлено, что ключевую патогенетическую роль играет не характер тератогенного фактора, а срок, на котором он «срабатывает»: чем раньше беременная женщина подвергается вредоносному воздействию, тем тяжелее последствия в плане развития бронхолегочной системы плода.
Диагностика сотрясения головного мозга
В больнице ребенка осматривает детский невропатолог, нейрохирург или травматолог. Он тщательно выясняет жалобы, собирает анамнез (историю заболевания), проводит общий и неврологический осмотр. Назначаются дополнительные методы диагностики. Основными являются рентгенография черепа, нейросонография (у маленьких детей), эхо-энцефалография (Эхо-ЭГ). При необходимости — компьютерная томография головного мозга (КТ), магниторезонансная томография (МРТ), электроэнцефалография (ЭЭГ), люмбальная пункция.
Рентгенография черепа проводится большей части больных. Целью данного исследования является выявление переломов черепа. Наличие любого повреждения костей черепа автоматически переводит травму в разряд средне-тяжелых или тяжелых (в зависимости от состояния ребенка). Иногда у маленьких детей с благополучной клинической картиной на рентгенограммах выявляются линейные переломы костей черепа. Судить о состоянии вещества головного мозга по рентгенограммам нельзя.
Нейросонография (НСГ) — это ультразвуковое исследование головного мозга. На нейросонограммах хорошо видно вещество головного мозга, желудочковая система. Можно выявить признаки отека головного мозга, очаги ушиба, кровоизлияний, внутричерепные гематомы. Процедура проста, безболезненна, быстро выполняется, не имеет противопоказаний. Ее можно проводить многократно. Единственное ограничение нейросонографии — наличие так называемых «естественных ультразвуковых окон» — большого родничка или тонких височных костей. Метод очень эффективен у детей в возрасте до 2 лет. Позже ультразвук становится трудно проходить через толстые кости черепа, что резко ухудшает качество изображения. Аппаратура для выполнения нейросонографии имеется в большинстве детских больниц.
Эхо-энцефалография (Эхо-ЭГ) — это также ультразвуковой метод исследования, который позволяет выявить смещение структур средней линии головного мозга, что может свидетельствовать о наличии дополнительных объемных образований головного мозга (гематомы, опухоли), дать косвенную информацию о состоянии вещества головного мозга и желудочковой системе. Метод этот простой и быстрый, однако надежность его невысока. Раньше он широко использовался в нейротравматологии, но при наличии современных средств диагностики, таких, как нейросонография, компьютерная и магниторезонансная томография, от него можно полностью отказаться.
Идеальным методом диагностики повреждений и заболеваний головного мозга является компьютерная томография (КТ). Это рентгенологический метод исследования, при котором с высокой четкостью можно получить изображения костей черепа и вещества головного мозга. По КТ диагностируются практически любые повреждения костей свода и основания черепа, гематомы, очаги ушиба, кровоизлияния, инородные тела полости черепа и пр. Точность этого исследования очень высока. Его основным недостатком является то, что КТ-аппарат дорог, и он есть далеко не в каждой больнице.
Магниторезонансная томография (МРТ) — наиболее точный, но сложный и дорогой метод обследования центральной нервной системы. Он редко используется для диагностики острой черепно-мозговой травмы, так как не позволяет увидеть кости черепа, менее точен для распознавания острых кровоизлияний, занимает больше времени, чем компьютерная томография, часто требует наркоза при обследовании маленьких детей — ребенок должен лежать абсолютно неподвижно в течение 10-20 минут, а маленькие дети этого сделать не могут; кроме того очень немногие клиники могут похвастаться наличием магниторезонансных томографов.
Электроэнцефалография (ЭЭГ) позволяет изучить биоэлектрическую активность головного мозга. Она применяется по специальным показаниям для оценки степени тяжести черепно-мозговой травмы, выявления очагов эпилептической активности. Очаг эпиактивности — область коры головного мозга с патологически измененной активностью нейронов (нервных клеток), которая может приводить к возникновению эпилептических приступов.
Люмбальная пункция — это забор ликвора (жидкости, омывающей головной и спинной мозг) из спинно-мозгового канала на поясничном уровне. Изменения в ликворе могут свидетельствовать о травме или кровоизлиянии (наличии крови) или воспалительном процессе, менингите. Люмбальная пункция проводится крайне редко и только по особым показаниям.
Терапия односторонней агенезии почки
Большинство детей, у которых отсутствует только одна почка, не имеют других симптомов, поскольку этот орган становится достаточно большим, чтобы выполнять функции обоих. Однако дети с односторонней агенезией почки могут иметь гипертензию (высокое кровяное давление). Им рекомендуется наблюдаться у педиатра.
Лечение при осложнениях:
- Пиелонефрит. Назначаются: постельный режим, специальная диета, антибиотикотерапия. Больным выписываются пенициллин, цефалоспорины 3, фторхинолоны, аминогликозиды. Терапия включает инфузионную терапию, детоксикацию с помощью плазмафереза, гемосорбции.
- Нефролитиаз. Камни удаляются малотравматичными эндоскопическими методами. Иногда применяются дистанционная литотрипсия и лапароскопия.
- Почечная недостаточность. В критическом состоянии больному требуется гемодиализ. В терминальной стадии проводят трансплантацию органа.